非洲猪瘟病毒通过带毒猪(康复猪)传播
Transmission of African Swine Fever virus via carrier (survivor) pigs does occur
作者:P.L. Ebléa*, T.J. Hagenaarsa, E. Weesendorpa, S. Quaka, H.W. Moonen-Leusena, W.L.A. Loeffena
a Wageningen Bioveterinary Research (WBVR), P.O. Box 65, 8200 AB Lelystad, The Netherlands
来源:Vet Microbiol. 2019 Oct;237:108345.
翻译:广州中农大生物科技有限公司 吴芷慧
重点:
ASFV Netherlands ’86毒株的康复猪可以将病毒传播给接触猪,导致急性感染
传播参数β带毒猪、感染周期T带毒猪和△R0的量化
无法说明ASFV污染环境对接触猪的感染效果
摘要:
本文探究从ASFV Netherlands ’86毒株急性感染中完全恢复的带毒猪是否可以通过直接接触传播将疾病传播给阴性猪。为此,我们使用了从ASFV感染中存活下来的猪。这些猪在临床上已经康复,并成为了ASFV带毒者。将这些临床健康的ASFV带毒猪与阴性猪一对一放在一起。12头阴性猪中有2头出现急性ASFV感染。根据实验结果,我们量化了传播参数β带毒猪(0.0039/天)和T带毒猪 (25.4天)。由于该ASFV毒株的存活率为0.3,转化为带毒猪对猪群R0的加权为0.3。此外,我们将阴性接触猪置于ASFV污染的环境中,但没有观察到环境接触感染。我们的研究结果表明,临床健康的ASFV带毒猪可能是新发感染的其中一个来源,并导致ASFV在猪群中的持续存在。我们估计的传播参数可用于建立家猪传播模型,并在一定程度上可用于建立野猪传播模型。
关键词:
非洲猪瘟、传播、幸存者、带毒者、环境、再生数
1. 介绍
非洲猪瘟(African Swine Fever, ASF)是一种高度传染性病毒疾病,由非洲猪瘟病毒科(Asfarviridae)的非洲猪瘟病毒(African Swine Fever Virus, ASFV)引起。许多感染了ASFV的猪病死,但如果猪从ASF感染中恢复(幸存猪),ASFV可在幸存猪(带毒猪)的组织或血液中持续存在较长时间,而带毒猪可能会导致病毒传播。ASFV带毒猪在疾病传播中的作用尚未清楚。此外,被ASFV感染猪污染的环境在ASFV传播途径中的作用同样还不清楚。了解哪些途径在ASF的传播中起作用,有助于建立ASFV的流行病学并制定有效的防控措施。估计不同传播路径的ASF传播参数对建立可以用于预测ASFV传播的模型或对防控措施效果的模拟至关重要。
在本研究中,我们探究了从ASFV Netherlands ’86毒株急性感染中完全康复的带毒猪是否会通过直接接触将ASFV传播给阴性猪,以及被ASFV感染猪污染的环境是否会导致接触猪感染。根据研究结果,我们量化了带毒猪带毒期的病毒传播率和感染周期,并探讨了总R0的分量。这些估值可直接用于建立家猪ASFV传播的模型。我们讨论了如何用这些估计值建立野猪ASFV传播的模型。
3 结果
3.1 临床症状
在直接接触传播实验中,带毒猪和C1猪均未见临床症状。2只C2猪(圈b和c)出现非洲猪瘟的临床症状(C2圈b:发热;C2圈c:发热,活力减退,皮肤发红)。为了避免病毒的进一步传播,两只猪都在47 dpi时被执行安乐死。
在间接接触传播实验中没有观察到临床症状。
3.2 qPCR、病毒分离和血清学实验结果
在直接接触传播试验中,在整个试验期间,带毒猪的OPF样本qPCR检测呈阳性,滴度处于恒定水平(1-3 10log TCID50-eq)。血液样本qPCR检测同样呈阳性,其中4头带毒猪的血液样本在整个检测期间呈阳性,2头的血液样本在第49天和第52天由阳性转阴性;3头猪血液样本的qPCR滴度处于恒定的高水平(5-6 10log TCID50-eq/ml,圈a、b、c),其他3头猪血液样本的qPCR滴度起始水平高但在测试期间逐步下降(图1)。大部分qPCR阳性样本在病毒分离中呈阳性(表1)。C1猪的血液和OPF样本qPCR和病毒分离检测结果均为阴性 (表1)。出现临床症状的C2猪(圈b、c)血液和OPF样本qPCR和病毒分离检测结果为阳性。滴度大于2 10log TCID50-eq 的时间点分别是47天(圈b)和45天(圈c)。其余4只C2猪的qPCR和病毒分离检测结果均为阴性(表1)。
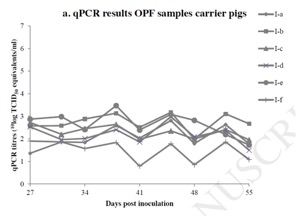
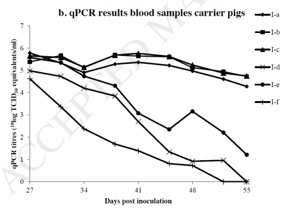
图1 带毒猪OPF拭子样本和血液样本的qPCR检测结果
表1 直接接触实验猪OPF拭子样本和血液样本的qPCR检测结果
OPF拭子
圈 | 猪 | dpi | ||||||||||||||||||||
27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 38 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 52 | 55 | ||
A | I | 1.36 | 1.9 | 1.8 | 2.6 | 2.0 | 2.8 | 1.8 | 2.6 | 1.8 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
B | I | 2.6 | 2.6 | 2.9 | 3.1 | 2.5 | 3.2 | 2.0 | 3.1 | 2.7 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | 0.7 | † | |||||||||||||||
C | I | 2.7 | 2.2 | 2.5 | 2.6 | 2.0 | 2.4 | 2.0 | 2.4 | 2.0 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | 2.0 | 3.9 | 3.7 | † | |||||||||||||||
D | I | 2.5 | 2.0 | 2.0 | 2.4 | 1.9 | 3.0 | 2.1 | 2.4 | 1.5 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
E | I | 2.9 | 3.0 | 2.4 | 3.5 | 2.4 | 3.1 | 2.8 | 2.2 | 1.7 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
F | I | 1.9 | 1.9 | 1.6 | 1.8 | 0.8 | 1.8 | 0.9 | 1.9 | 1.1 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
血液样本
圈 | 猪 | dpi | ||||||||||||||||||||
27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 38 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 52 | 55 | ||
A | I | 5.8a,b | 5.3 | 4.9 | 5.3 | 5.4 | 5.2 | 5.0 | 4.6 | 4.3 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
B | I | 5.4 | 5.7 | 5.1 | 5.7 | 5.6 | 5.6 | 5.1 | 4.9 | 4.7 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | 1.2 | 5.8 | † | |||||||||||||||
C | I | 5.7 | 5.6 | 5.1 | 5.7 | 5.8 | 5.6 | 5.2 | 4.9 | 4.7 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | 6.9 | 7.2 | 7.2 | † | |||||||||||||||
D | I | 5.0 | 4.7 | 4.2 | 3.9 | 2.7 | 1.3 | 0.9 | 1.0 | - | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
E | I | 5.6 | 5.4 | 4.7 | 4.3 | 3.1 | 2.4 | 3.2 | 2.2 | 1.2 | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
F | I | 4.6 | 3.4 | 2.4 | 1.7 | 1.4 | 0.8 | 0.7 | - | - | ||||||||||||
C1 | - | - | - | - | - | - | - | - | - | - | ||||||||||||
C2 | - | - | - | - | - | inc | - | - | - | - | ||||||||||||
a qPCR滴度(10log TCID50-eq/ml);- = 阴性
b 加粗下划线 = 病毒分离呈阳性
c 无定论,样本qPCR检测呈阳性但没有感染特征,认为是假阳性。
在间接接触传播实验中,圈I、II、IV采集的地板样本在qPCR中检测为(弱)阳性(qPCR结果为-0.7 -2.4 10log TCID50 eq/ml)。在所有猪都因急性ASF感染而死亡或安乐死的圈I采集的多个样本中,28-45 dpi的样本检测呈阳性。圈II、IV抽取的样本偶有阳性。圈III没有分离到病毒,且有3头感染猪存活。圈I、IV在45 dpi分离到病毒,分别对应于各圈中最后一批猪被移出后的第32天和18天。圈I(2头)和圈II(1头)中IC猪的OPF样本,尤其是来自圈I的样本,在几次qPCR中检测为弱阳性(0.7-1 10log TCID50 eq/ml)。但无法从这些阳性的地板拭子和OPF样本中分离出活病毒(表2)。IC猪的血液样本在qPCR中检测均为ASFV阴性(结果未展示)。
直接和间接传播实验中收集的空气样本在qPCR和病毒分离中检测均为阴性(结果未展示)。
27和55 dpi的带毒猪血清样本ASFV抗体检测为阳性。接触实验开始时(27 dpi)阻断比是70%-90%。接触实验结束时(55 dpi)阻断比非常接近,为99%-101%。
表2 间接接触实验环境样本和IC哨兵猪OPF拭子样本qPCR检测结果
dpi | ||||||||||||||
圈 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 38 | 40 | 42 | 45 | ||
I | 地板样本 | 1 | 1.17a | 1.3 | 1.3 | 0.8 | - | 0.4 | ||||||
2 | - | 2.4 | 0.8 | 0.6 | - | - | ||||||||
3 | 1.4 | 1.1 | - | 1.1 | - | - | ||||||||
4 | 1.5 | 1.4 | 1.1 | 1.1 | - | - | ||||||||
IC猪OPF | ICa | 0.7 | 0.8 | - | - | - | - | - | - | - | - | - | ||
ICb | - | 0.9 | 0.8 | 1.0 | - | - | - | - | - | - | - | |||
II | 地板样本 | 1 | - | - | 0.4 | - | - | - | ||||||
2 | 0.8 | - | 0.2 | - | - | - | ||||||||
3 | - | 0.8 | - | - | - | - | ||||||||
4 | -0.7 | - | - | 0.6 | - | - | ||||||||
IC猪OPF | ICa | - | - | - | - | - | - | - | - | - | - | - | ||
ICb | - | 0.8 | - | - | - | - | - | - | - | - | - | |||
III | 地板样本 | 1 | - | - | - | - | - | - | ||||||
2 | - | - | - | - | - | - | ||||||||
3 | - | - | - | - | - | - | ||||||||
4 | - | - | - | - | - | - | ||||||||
IC猪OPF | ICa | - | - | - | - | - | - | - | - | - | - | - | ||
ICb | - | - | - | - | - | - | - | - | - | - | - | |||
IV | 地板样本 | 1 | - | - | - | - | - | 1.2 | ||||||
2 | - | 0.4 | - | - | - | - | ||||||||
3 | - | 0.6 | - | - | 0.4 | - | ||||||||
4 | - | - | - | - | 0.4 | - | ||||||||
IC猪OPF | ICa | - | - | - | - | - | - | - | - | - | - | - | ||
ICb | - | - | - | - | - | - | - | - | - | - | - | |||
a qPCR滴度(10log TCID50-eq/ml);- = 阴性
所有qPCR阳性样本在病毒分离检测中均为阴性
3.3 接触感染和传播参数的量化
3.3.1 接触传染
在直接接触传播实验中,C1猪均未感染,C2猪有2头感染。估计2头C2猪的感染日分别为42dpi,即接触后1天(猪圈c)和44dpi,即接触后3天(猪圈b)。出现接触传播的带毒猪血液中病毒水平很高(图1)。C1组和C2组之间的接触感染数量没有显著差异(p=0.5, Fisher精确检验)。接触感染的发生时间分布均匀(p=0.5,卡方检验),未发现接触感染发生时间上的聚类。
3.3.2 传播参数的量化
表3中总结了β带毒猪和T带毒猪 的估计值和95%置信区间,并估计了ASFV Netherlands ’86毒株急性阶段的传播参数。
28-41 dpi(C1猪)时期的传播参数β带毒猪为0/天,42-55 dpi(C2猪)时期的为0.093/d,试验全程28-55 dpi的β带毒猪 =0.039/d。本实验估计的平均传染期T带毒猪 为25.4 d。感染周期估计的起始点是28 dpi。整个带毒期的M是0.039×25.4=0.99。在我们研究中,成为带毒猪的可能性是0.3(6/20)。ΔR0 是0.3×0.99=0.3。
表3 ASFV传播速率参数

因此我们的结论是,临床健康的ASFV幸存猪成为带毒猪后可将ASFV传播给阴性接触猪,传播能力取决于带毒猪的存活率和带毒持续时间。我们估计的传播参数适用于家猪ASFV传播模型,部分适用于野猪模型。










